Hoe bereken je de bronspanning?
In een elektrochemische cel zullen de processen (en dus ook de stroom) pas op gang komen als voldaan is aan de eis dat het verschil tussen de standaardelektrodepotentiaal van de oxidator en de standaardelektrodepotentiaal van de reductor meer dan 0,3 Volt bedraagt. Met andere woorden:
V0(ox) − V0(red) ≥ 0,3 V
Laten we eens kijken naar onderstaande elektrochemische cel. In de linker halfcel bevindt een Zn elektrode zich in een oplossing van zinksulfaat (0,1 M). Rechts bevindt zich een Cu elektrode in een oplossing van kopersulfaat (0,1 M).
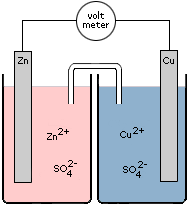
De halfreacties die hier optreden zijn:
Zn(s)\(\rightleftarrows\)Zn2++2 e−![]() voor de halfcel met de reductor
voor de halfcel met de reductor
Cu2++2 e−\(\rightleftarrows\)Cu (s)![]() voor de halfcel met de oxidator
voor de halfcel met de oxidator
Door toepassing van de Wet van Nernst weten we dat de halfcel met de reductor een potentiaal heeft van −0,79 V en de halfcel met de oxidator een potentiaal van +0,31 V heeft.
De spanning die deze elektrochemische cel kan opwekken (ook wel de bronspanning V genoemd) is het potentiaalverschil tussen de elektrodepotentiaal van de halfcel van de oxidator en de elektrodepotentiaal van de halfcel van de reductor.
ΔV = VOX − VRED
De bronspanning van bovenstaande cel is dus:
ΔV = 0,31 − (−0,79) = 1,10 V.