Wat is een atomaire stof?
Atomaire stoffen zijn stoffen waarbij de atomen door sterke atoombindingen zijn verbonden tot een continu netwerk. Atomaire stoffen hebben een atoomrooster. Omdat atomaire stoffen zijn verbonden tot een netwerk bestaan ze dus niet uit losse moleculen.
Enkele voorbeelden zijn:
- diamant (heeft een driedimensionaal netwerk van koolstofatomen)
- grafiet (heeft tweedimensionale lagen van koolstofatomen)
- siliciumdioxide
- wolfraamcarbide
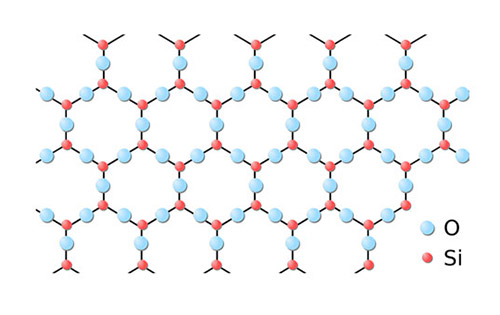 |
| Schematische weergave van het atoomrooster bij siliciumdioxide (kwarts). |
Eigenschappen
Omdat er bij atomaire stoffen geen sprake is van vrij bewegende elektronen, geleiden de stoffen geen elektrische stroom. Een uitzondering hierop vormt grafiet dat wel stroom geleidt.
Door de aanwezigheid van atoombindingen hebben atomaire stoffen een zeer hoog smeltpunt. De bindingen zorgen ook voor een sterke hardheid. Uitzondering hierop is wederom grafiet waarbij de lagen gemakkelijk langs elkaar heen kunnen schuiven waardoor de stof vervormbaar is.
Atomaire stoffen zijn over het algemeen onoplosbaar in elk oplosmiddel.